1 września 2019 roku na listę leków refundowanych dostępnych w ramach programu lekowego trafił nowolumab. Oznacza to, że immunoterapia nowotworów głowy i szyi będzie dostępna dla polskich chorych spełniających wymagania opisane w programie lekowym dotyczącym niwolumabu w leczeniu płaskonabłonkowego raka jamy ustnej, gardła lub krtani postępującego podczas lub po zakończeniu terapii opartej na pochodnych platyny (ICD-10 C01, C02, C03, C04, C05, C06, C09, C10, C12, C13, C14, C32).
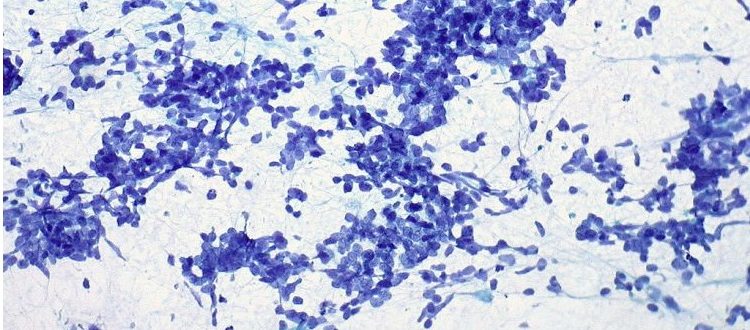
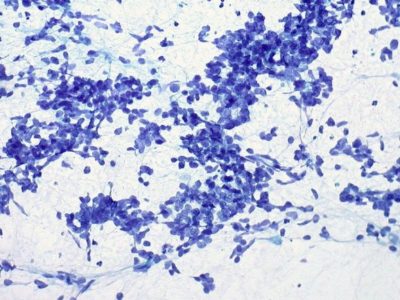
Nowotwory regionu głowy i szyi
Według danych Krajowego Rejestru Nowotworów – nowotwory regionu głowy i szyi stanowią w Polsce 9% wszystkich nowotworów rozpoznanych u mężczyzn i 5% u kobiet. Raki narządów głowy i szyi są częstsze u osób po 45 roku życia, natomiast nowotwory rozwijające się jako efekt infekcji wirusem brodawczaka ludzkiego HPV występują u młodszych osób.
Zdecydowaną większość nowotworów tej lokalizacji rozpoznaje się w zaawansowanym stadium klinicznym. U połowy pacjentów po leczeniu radykalnym dochodzi do wznowy procesu nowotworowego lub wystąpienia przerzutów odległych. Nadzieję na poprawę wyników leczenia nowotworów regionu głowy i szyi dają doniesienia z badań klinicznych potwierdzające skuteczność immunoterapii w tym wskazaniu.
Immunoterapia nowotworów głowy i szyi w postaci cząsteczek niwolumab i pembrolizumab została zarejestrowana przez Amerykańską Agencję ds. Żywności i Leków (FDA) oraz Komisję Europejską.
Cząsteczka immunokompetentna niwolumab (refundowana w Polsce w leczeniu czerniaka, raka płuca, nerki i chłoniaka Hodgkina) otrzymała również pozytywną rekomendację Prezesa Agencji Ochrony Technologii Medycznych i Taryfikacji we wskazaniu leczenie dorosłych pacjentów z nawrotowym lub przerzutowym płaskonabłankowym rakiem jamy ustnej, gardła lub krtani.
Immunoterapia niwolumabem – decyzją Ministerstwa Zdrowia – trafiła do refundacji (w ramach programu lekowego) i jest dostępna w Polsce od 1 września 2019 roku.
– Cząsteczka, która uzyskała pozytywną opinię AOTM – niwolumab, jest zarejestrowana w terapii płaskonabłonkowych nowotworów głowy i szyi w przypadku choroby nawrotowej lub przerzutowej po progresji podczas lub po zakończeni terapii cisplatyną. Badanie na podstawie którego zarejestrowano niwolumab wykazało korzyść w zakresie mediany przeżycia całkowitego (OS – overall survival). Mediana OS w grupie pacjentów otrzymujących niwolumab wynosiła 7,5 miesiąca, natomiast osoby otrzymujące chemioterapię miały raportowaną medianę OS 5,1 miesiąca – wyjaśnia lek. Izabela Łasińska.
Leczenie nowotworów regionu głowy i szyi
Nowotwory okolicy głowy i szyi stanowią istotny problem medyczny, ponieważ dotyczą ważnej okolicy ludzkiego ciała. Rozwój nowotworów narządu głowy i szyi może utrudniać choremu oddychanie, odżywianie, prowadzić do zaburzenie mowy, upośledzenia wzroku, słuchu, węchu , smaku czy mimiki twarzy. Pod pojęciem nowotwory okolicy głowy i szyi rozumie się najczęściej nowotwory złośliwe jamy ustnej, gardła, krtani, jamy nosowej, gruczołów ślinowych i zatok obocznych nosa.
U pacjentów z nowotworami okolicy głowy i szyi postępowanie lecznicze zależy od umiejscowienia nowotworu, stadium zaawansowania klinicznego choroby, rozpoznania histopatologicznego oraz wieku, stanu sprawności i stanu odżywienia chorego.
Głównymi metodami leczenia radykalnego są chirurgia onkologiczna i/lub radioterapia. Często stosuje się kojarzenie tych metod. W bardziej zaawansowanych przypadkach napromienianie kojarzone jest także z jednoczesną chemioterapią.
W przypadku choroby ogólnoustrojowej rzadko występują sytuacje, w których możliwe jest zastosowanie leczenia chirurgicznego lub radioterapii. U większości chorych jedyną metodę leczenia stanowi chemioterapia stosowana przede wszystkim w celu uzyskania lepszej jakości życia. Wśród cytostatyków wykorzystywanych w leczeniu zaawansowanych nowotworów regionu głowy i szyi znajdują się cisplatyna, taksoidy, metotreksat, ifosfamid, bleomycyna i fluorouracyl.
Nową jakoś w onkologii stanowi immunoterapia, która znalazła zastosowanie również w leczeniu chorych na raka narządu głowy i szyi. Dane z przeprowadzonych badań klinicznych potwierdziły, że immunoterapia w tym wskazaniu jest najbardziej skuteczna w przypadku nawrotów lub przerzutów odległych, które są oporne na standardową chemioterapię. Dwa leki (niwolumab i pembrolizumab) posiadają już rejestrację FDA i EMA. Jeden z nich – niwolumab – trafił na listę refundacyjną i jest dostępny dla pacjentów w Polsce od 1 września 2019 roku.
Immunoterapia nowotworów głowy i szyi
– Immunoterapia nowotworów polega na uzyskaniu odpowiedzi układu odpornościowego organizmu po zastosowaniu np. przeciwciał i rozpoznawaniu komórek nowotworowych jako „obce” oraz niszczeniu ich przez układ immunologiczny. Niwolumab to przeciwciało monoklonalne łączące się z receptorem programowanej śmierci (PD-1) i blokujące jego oddziaływanie z ligandem PDL-1. Receptor PD-1 to negatywny regulator limfocytów T, hamujący ich działanie. Połączenie PD-1 z PDL-1 – obecnymi na komórkach nowotworowych lub komórkach występujących w mikrośrodowisku guza – skutkuje zahamowaniem namnażania limfocytów T oraz zmniejszeniem produkcji cytokin. Dzięki zastosowaniu niwolumabu dochodzi do zablokowania połączenia receptora z ligandem, co w konsekwencji nasila odpowiedź immunologiczną i prowadzi do niszczenia komórek nowotworowych przez organizm pacjenta – tłumaczy lek. Izabela Łasińska.
W kwietniu 2017 roku Komisja Europejska zarejestrował cząsteczkę immunokompetentną niwolumab w monoterapii płaskonabłonkowego raka głowy i szyi (SCCHN) u dorosłych pacjentów, u których nastąpiła progresja choroby w trakcie lub po leczeniu preparatami na bazie platyny. Rejestracji dokonano na podstawie wyników badania CheckMate-141, globalnego, otwartego badania klinicznego fazy 3 z randomizacją, opublikowanego w The New England Journal of Medicine w październiku 2017 roku. Była to pierwsza w Europie rejestracja leku w leczeniu płaskonabłonkowego raka głowy i szyi od ponad dekady.
Jak informuje New England Journal of Medicine – działająca na układ odpornościowy cząsteczka immunokompetentna niwolumab ponad dwukrotnie wydłuża okres przeżycia pacjentów z zaawansowanymi nowotworami głowy i szyi.
Podczas badań klinicznych z udziałem ponad 350 pacjentów leczonych niwolumabem chorzy z nowotworami głowy i szyi mieli większe szanse na dłuższe przeżycie w porównaniu z grupą kontrolną, leczoną standardową chemioterapią. Po roku pozostało przy życiu 36 proc. leczonych lekiem immunoterapeutycznym – wobec 17 proc. leczonych chemioterapią. Immunoterapia powodowała także mniej skutków ubocznych niż chemioterapia. Korzyści z leczenia immunologicznego były szczególnie widoczne u pacjentów z dodatnim wynikiem testów na obecność wirusa HPV.
Niwolumab w leczeniu raka narządu głowy i szyi – program lekowy
Niwolumab w leczeniu płaskonabłonkowego raka jamy ustnej, gardła lub krtani postępującego podczas lub po zakończeniu terapii opartej na pochodnych platyny (ICD-10 C01, C02, C03, C04, C05, C06, C09, C10, C12, C13, C14, C32) jest refundowany od 1 września 2019 roku.
Kryteria kwalifikacji do leczenia (powinny zostać spełnione łącznie):
- Histologicznie potwierdzony płaskonabłonkowy nowotwór jamy ustnej, gardła lub krtani;
- Udokumentowane wcześniejsze leczenie oparte na pochodnych platyny;
- Stwierdzony nawrót (miejscowy lub węzłowy) lub uogólnienie (przerzuty) stwierdzone w trakcie lub w ciągu 6 miesięcy po zakończeniu wcześniejszej chemioterapii z udziałem jednej z pochodnych platyny;
- Sprawność w stopniu 0-1 wg klasyfikacji WHO lub ECOG;
- Brak aktywnych chorób autoimmunologicznych z wyłączeniem cukrzycy typu I, niedoczynności tarczycy (leczonej wyłącznie suplementacją hormonalną), łuszczycy, bielactwa;
Czas leczenia w programie określa lekarz. Leczenie należy kontynuować tak długo, dopóki obserwuje się korzyści kliniczne a leczenie jest tolerowane przez pacjenta.
Źródła:
www.nejm.org/doi/full/10.1056/NEJMoa1602252#t=article
http://bipold.aotm.gov.pl/assets/files/zlecenia_mz/2018/044/REK/RP_56_Opdivo_2018-KW.pdf
www.oncology-central.com/2016/04/21/aacr16-nivolumab-demonstrates-significant-survival-benefit-in-advanced-head-neck-cancer/
http://dziennikmz.mz.gov.pl/